تست اپسیلومتر (Etest) – اصول، روش، نتایج و مزایا
بررسی مقاومت میکروارگانیسمهای مختلف نسبت به دارو و انتیبیوتیک در علم پزشکی و درمان بیماران از اهمیت بالایی برخوردار است. از همین رو، محققین در آزمایشگاهها با استفاده از روشهای مختلفی میزان حساسیت و مقاومت یک ارگانیسم را نسبت به داروهای مختلف میسنجند و بنابر نتایج بهدست آمده به توسعه روشهای درمانی میپردازند. تست اپسیلومتر [1] یکی از این روشها است.
تست اپسیلومترکه اغلب با نام Etest شناخته میشود روشی برای تعیین حساسیت یک ارگانیسم نسبت به عوامل ضدمیکروبی است که با قرار دادن یک نوار آغشته به مواد ضد میکروبی روی یک پلیت آگار انجام میشود.
به کمک این تست میتوان به پزشکان نشان داد که چه غلظتی از داروهای ضد میکروبی میتواند با موفقیت برای درمان بیماران استفاده شود.
از آنجایی که این موضوع بسیار برای سلامت عمومی حائز اهمیت است، در ادامهی این مطلب قصد داریم به بررسی تست اپسیلومتر (Etest)، روش انجام ان و نتایج ناشی از آن بپردازیم. لازم به ذکر است که در این مطلب، اغلب از نام اختصاری تست اپسیلومتر، یعنی E test استفاده شده است.
مروری اجمالی بر Etest
نوار Etest اولین بار در سال 1988 توصیف شد و در سال 1991 توسط شرکت AB BIODISK به صورت تجاری معرفی شد. شرکت bioMérieux در سال 2008، AB BIODISK را خریداری کرد و به تولید و عرضه نوار Etest تحت علامت تجاری Etest ادامه داد.
در طول دهه 1950، هانس اریکسون (Hans Ericsson) (استاد میکروبیولوژی و بنیانگذار علمی شرکت AB BIODISK، روشی را برای استاندارد کردن تست انتشار دیسک (disk diffusion) و بهبود تکرارپذیری و قابلیت اطمینان این روش توسعه داد.
در این روش که همان Etest است، هم از رقیق کردن آنتی بیوتیکها و هم انتشار (دفیوژن [2]) آنتی بیوتیکها در محیط استفاده شد. اگر بخواهیم دقیقتر بگوییم، در این آزمایش یک الگوی دیسک دفیوژن (disk diffusion) با روش تعیین حداقل غلظت بازدارنده[3] (MIC) ترکیب میشود. حداقل غلظت بازدارنده کمترین غلظت یک مادهی ضد میکروبی در نظر گرفته میشود که رشد مرئی یک میکروارگانیسم را مهار میکند.
Etest برای اولین بار در کنفرانس علوم (Interscience Conference) در سال 1988 معرفی شد. در این کنفرانس که در رابطه با عوامل ضد میکروبی و شیمی درمانی (ICAAC) در لس آنجلس برگزار گردید، Etest به عنوان یک مفهوم جدید برای تعیین حداقل غلظت بازدارنده ارائه شد. در سپتامبر 1991، Etest پس از دریافت مجوز از سازمان غذا و داروی ایالات متحده (FDA) به عنوان یک محصول مناسب برای تعیین حداقل غلظت بازدارنده در سطح جهانی معرفی گردید.
اصول و کاربردهای Etest
در Etest، از نوارهای پلاستیکی مستطیلی استفاده میشود. یک طرف نوار Etest آغشته به غلظتی از عامل ضد میکروبی است و طرف دیگر نوار حاوی یک مقیاس عددی است.
نوار Etest دارای طیف گستردهای از ( بیش از 100) مرجع ضد میکروبی است که میتوان آنها را به 4 دستهی زیر طبقه بندی کرد:
- آنتی بیوتیکها
- عوامل ضد قارچی
- عوامل ضد مایکوباکتری
- تست فنوتیپ مقاومت (Resistance phenotype testing)
برای بررسی مقاومت یا حساسیت میکروارگانیسم نسبت به یک داروی خاص، ابتدا سوسپانسیون باکتریایی، با استفاده از سواب استریل، روی آگار کشت داده میشود.
سپس نوار Etest روی پلیت آگار تلقیح شده، قرار میگیرد.
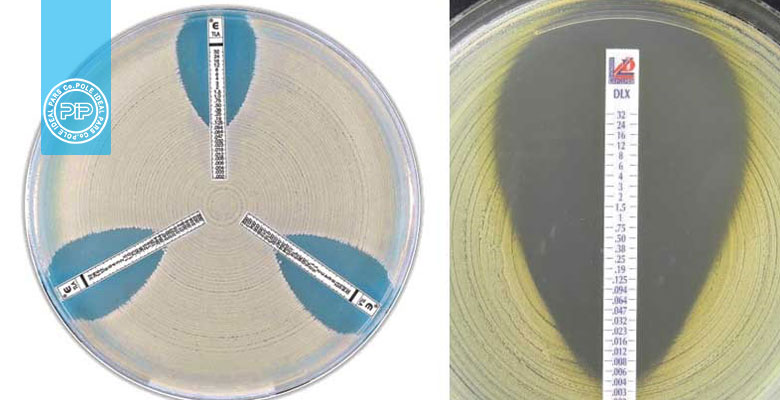
پس از قرار دادن نوار روی سطح آگار، بلافاصله آنتی بیوتیکها از سطح حامل پلاستیکی به سطح آگار آزاد میشوند. پس از انکوباسیون، رشد باکتری در پلیت قابل مشاهده است و بیضی مهار در طول نوار دیده میشود. حداقل غلظت بازدارنده ( بر حسب میکروگرم بر میلی لیتر) در جایی مشخص میشود که لبه بیضی مهار، نوار را قطع میکند. (مانند شکل 1)

از Etest برای اهداف زیر استفاده میشود:
1. یکی از کاربردهای مهم تست اپسیلومتر، تعیین حداقل غلظت بازدارنده (MIC) برای میکروارگانیسمها است. همانطور که قبلا نیز گفته شد، حداقل غلظت بازدارنده، کمترین غلظت یک مادهی ضد میکروبی در نظر گرفته میشود که رشد یک میکروارگانیسم را مهار میکند.
به کمک تست اپسیلومتر میتوان این مقدار را برای ارگانیسمهای فستیدیوس (Fastidious)، ارگانیسمهای کند رشد (مانند مایکوباکتریومها) و همچنین ارگانیسمهایی که برای رشد به آگارهای مخصوص برای تغذیه نیاز دارند، محاسبه کرد.
2.از دیگر کاربردهای Etest میتوان به بررسی مقاومت فنوتیپی برای یک عامل ضد میکروبی خاص اشاره کرد. لازم به ذکر است که مقاومت آنتیبیوتیکی یک میکروارگانیسم، معمولاً با تغییرات ژنتیکی یا به دست آوردن ژنهای مقاوم به فعالیت آنتیبیوتیک مرتبط است. با این وجود، در برخی شرایط ارگانیسم قادر است مقاومت را بدون هیچ گونه تغییر ژنتیکی به دست آورد. این مقاومت، فنوتیپی نامیده میشود که به کمک تست اپسیلومتر میتوان آنرا بررسی نمود.
روش انجام Etest
۱. موارد احتیاط
- هنگام کار با نمونههای باکتریایی باید از روشهای آسپتیک و اقدامات احتیاطی در برابر خطرات میکروبیولوژیکی استفاده شود.
- آزمون باید دقیقاً مطابق با روشهای توصیف شده انجام شود.
- هنگام قرار دادن نوار Etest روی صفحه حاوی سوسپانسیون باکتریایی، باید بسیار مراقب باشید تا سطح آگار و لبه پلیت را لمس نکنید.
- نتایج را فقط در صورتی بخوانید که بیضی مهار کاملا قابل مشاهده باشد. (بیضی مهار در شکل 1 مشخص است)
- حین قرار دادن چندین نوار روی یک پلیت، نوارها نباید با یکدیگر تماس داشته باشند تا در تفسیر نتیجهی آنتی بیوتیک داده شده تفاوت ایجاد نشود.
۲. انتخاب آگار
Etest را میتوان با انواع مختلف آگار استفاده کرد. به شرطی که آگار انتخاب شده از رشد خوب ارگانیسمهای مورد آزمایش حمایت کند و با فعالیت عامل ضد میکروبی تداخل نداشته باشد.
با این وجود، برای به حداکثر رساندن تکرارپذیری، محیط انتخاب شده باید الزامات اساسی برای یک محیط تست حساسیت را برآورده کند.
در اغلب موارد آگارهای زیر برای استفاده در Etest توصیه میشوند:
- هوازی: مولر هینتون آگار (Mueller Hinton agar)
- بیهوازی: بروسلا بلاد آگار (Brucella blood agar) با مکملهای مناسب
این محیطها ممکن است به مواد مغذی مکمل نیاز داشته باشند تا رشد ارگانیسمهای سختگیر مانند پنوموکوک (pneumococci)، استرپتوکوک (streptococci)، ابیوتروفیا (Abiotrophia) و کمپیلوباکتر (Campylobacter) صورت گیرد.
۳. آمادهسازی تلقیح
- بسته Etest را حداقل 30 دقیقه قبل از آزمایش از فریزر (20- درجه سانتیگراد) خارج کنید.
- 3 یا 4 کلونی از سویههای آزمایشی را امولسیون کرده و آن را به یک لوله حاوی سالین منتقل کنید.
- میزان کدورت باید با استاندارد McFarland 0/5 مطابقت داشته باشد.
بر اساس استاندارد McFarland 0/5 ، چگالی سوسپانسیون باکتریایی به صورت زیر است:
1.5x 10^8 colony forming units (CFU/ml).

لازم به ذکر است که نوار استاندارد McFarland 0/5 به صورت تجاری در دسترس است.
۴. تلقیح در آگار
- یک سواب پنبهای استریل را به تلقیح آماده شده در بخش اول، آغشته کنید.
- با استفاده از تکنیک استریک پلیت یا کشت خطی و با زاویه تقریباً 60 درجه، سواب آغشته به تلقیح را روی تمام سطح آگار قرار دهید و خطوط زیگزاگی ایجاد کنید.
- درب پلیت حاوی آگار را به مدت 5 دقیقه ببندید تا رطوبت اضافی جذب شود.
۵. قرار دادن نوار Etest
- بسته Etest را باز کرده و با استفاده از فورسپس استریل، یک نوار بیرون بیاورید.
- با استفاده از فورسپس نوارها را روی سطح آگار قرار دهید. انتهای نوار باید با لبه ی پلیت تماس داشته باشد و مقیاس رو به بالا قرار گیرد تا قابل مشاهده باشد.
- پلیت را در دمای 37 درجه سانتیگراد به مدت 18 تا 24 ساعت انکوباسیون کنید.
بررسی نتایج
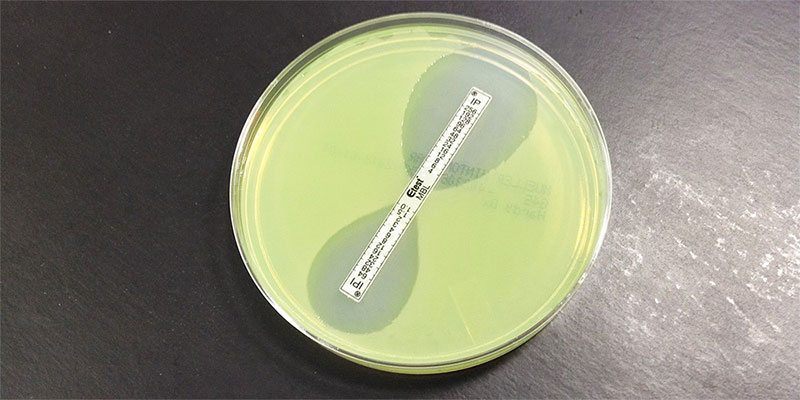
- پس از انکوباسیون، یک بیضی مهار روی پلیت دیده میشود.
- حداقل غلظت بازدارنده (MIC) در قسمت تقاطع قسمت پایینی بیضی مهار با نوار تست خوانده میشود.
- اگر مقدار MIC بین دو رقت باشد، همیشه عدد خوانده شده را تا بالاترین مقدار گرد کنید.
- مقادیر MIC باکتری باید به عنوان S (مستعد)، I (متوسط) یا R (مقاوم) تفسیر شوند.

مزایا و معایب استفاده از روش Etest
اجرای روش Etest بسیار آسان است و برای انجام آن به آموزش زیادی نیاز نیست. همچنین این روش چندان زمانبر نبوده و برای طیف وسیعی از داروها و میکروارگانیسمها قابل استفاده است.
اما روش Etest معایبی نیز دارد.
به عنوان مثال برای کریپتوکوکوس نئوفورمانس (Cryptococcus neoformans) مناسب نیست.
سخن پایانی
همانطور که در این مطلب خواندید، روش Etest یک روش کاربردی و تایید شده برای بررسی و تعیین میزان مقاومت میکروارگانیسمها نسبت به یک مادهی ضد میکروبی است که در علوم پزشکی و تشخیصی از اهمیت بالایی برخوردار است. در این مطلب سعی کردیم به بررسی این روش و نتایج حاصل از آن بپردازیم. امیدواریم این مطلب مورد توجه شما قرار گرفته باشد.
واژه نامه:
| Minimum Inhibitory Concentration | [3] | diffusion | [2] | Epsilometer test | [1] |






سلام. ایا امکان تهیه کیت های E-test برای قارچ ها اط طرف شرکت شما وجود دراد؟
سلام. ایا امکان تهیه کیت های E-test برای قارچ ها اط طرف شرکت شما وجود دراد؟
سلام خیر متاسفانه. ما تولید کننده لوزام پزشکی و ازمایشگاهی هستیم. برای اطلاع از محصولات می توانید وبسایت medpip.com را مشاهده نمایید.