
تشخیص سودوموناس آئروژینوزاهای بدون پیگمان
تهیه و تنظیم: دکتر محمد قهری
حدود 10 درصد از سویههای سودوموناس آئروژینوزا در جداسازی اولیه پیگمان تولید نمیکنند. در این موارد رشد در 42 درجه سانتیگراد و عدم رشد در 4 درجه سانتیگراد و توانایی احیای نیترات به گاز نیتروژن میتواند تشخیص سودوموناس آئروژینوزا را مطرح نماید.
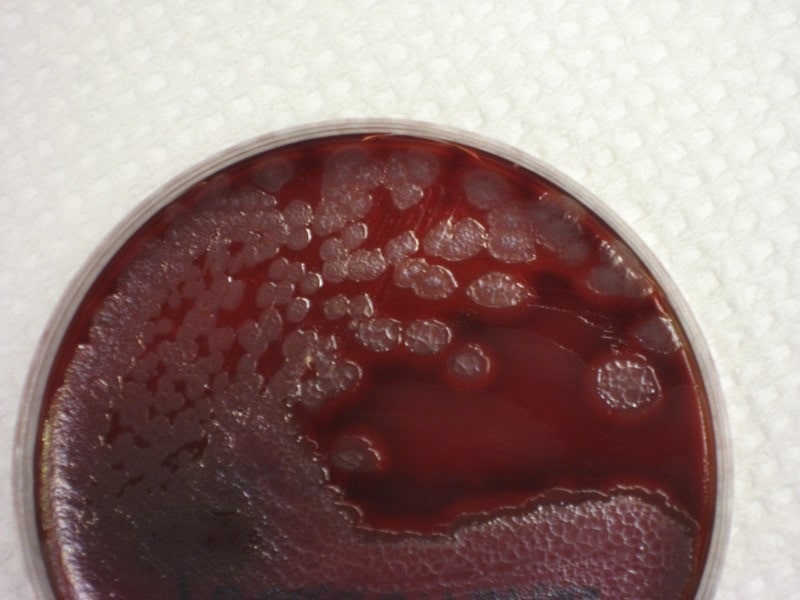
بررسی خصوصیات بیوشیمیایی
این باکتری قادر است با تولید آنزیمهای هیدرولیتیک، سوبستراهای مختلف را هضم کند. ژلاتین را بهسرعت ذوب کرده و آمونیاک تولید میکند، همچنین میتواند با تولید آنزیمهای لیپاز، لسیتیناز و اورهآز بهترتیب توئین 80، زرده تخممرغ و اوره را هیدرولیز کند، اما قادر به هیدرولیز نشاسته، پلی بتاهیدروکسی بوتریک اسید و ONPG نیست. بیشتر سویههای سودوموناس آئروژینوزا، گلوکز را در محیط پایه اکسید کرده و بدون ایجاد گاز اسید تولید میکنند. این باکتری همچنین قادر است این واکنش را در محیطهای حاوی فروکتوز، گالاکتوز، مانوز، رامنوز، گزیلوز و مانیتول انجام دهد. سودوموناس آئروژینوزا اورهآز، اکسیداز، کاتالاز و آرژینین دهیدرولاز مثبت است. لیزین دكربوكسیلاز، لاکتوز و اورنیتین دكربوكسیلاز منفی اسـت. ++ – – =IMViC و روی KIA و TSI بهصورت AIK/AIK است و H2S منفی است. بر روی محیط ژلوز خوندار همولیز کامل ایجاد میکند.
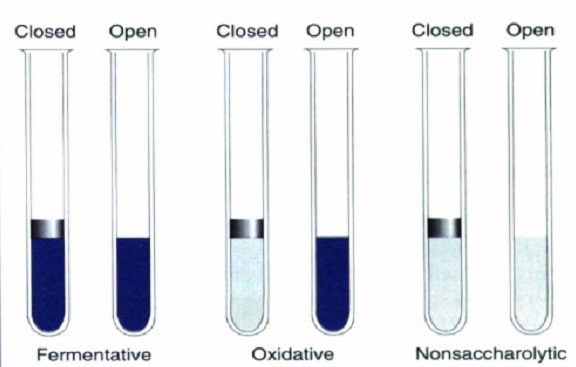
محیط O-F
سودوموناس آئروژینوزا دارای متابولیسم اکسیداتیو است و مهمترین راه متابولیسم گلوکز و سایر هگزوزها در این باکتری مسیر متابولیکی انترو-دئودوروف است و از اکسیداسیون قندها مقدار کمی آب و اسید تولید میکند. جهت بررسی تجزیه گلوکز میتوان از محیط Hugh & Leifson استفاده کرد. از طریق اکسیداسیون گلوکونات و تشکیل لعاب در این محیط، احیای نمکهای تترازولیوم و ایجاد کلنیهای قرمز، احیای سلنیت و دامیناسیون استامید، میتوان سودوموناس آئروژینوزا را از سایر سودوموناسهای فلورسنت تشخیص داد. این محیط حاوی 0/2 درصد پپتون و یک درصد قند (در انتروباكتریاسه به نسبت 2/1) بوده که كاهش پپتون جهت تشكیل محصولات اكسیداسیون از اسیدهای آمینه در نتیجه افزایش pH لازم است. کشت باکتری بر روی این محیط به شکل خطی و عمقی در دو لوله حاوی محیط کشت انجام میگیرد، سپس بر روی سطح یکی از لولهها به مقدار 2-1 سانتیمتر پارافین مایع استریل اضافه میگردد تا رشد باکتری در شرایط بیهوازی قرار گیرد، در صورتیکه لوله اولی در شرایط هوازی قرار دارد. چنانچه لوله کشت در شرایط هوازی زرد رنگ شد و لوله دومی بدون تغییر رنگ باقی ماند، باکتری هوازی بوده و گلوکز را اکسیده نموده است که از جمله خصوصیات سودوموناسها است و اگر لوله فاقد پارافین به رنگ آبی تغییر رنگ داد و لوله دارای پارافین بدون تغییر باقی ماند، نشانه اکسیداسیون پروتئینها بوده که از جمله صفات آلکالیژنز است. اگر هر دو لوله به رنگ زرد تغییر رنگ دادند نشاندهنده تخمیری بودن باکتری است (شکل 1).
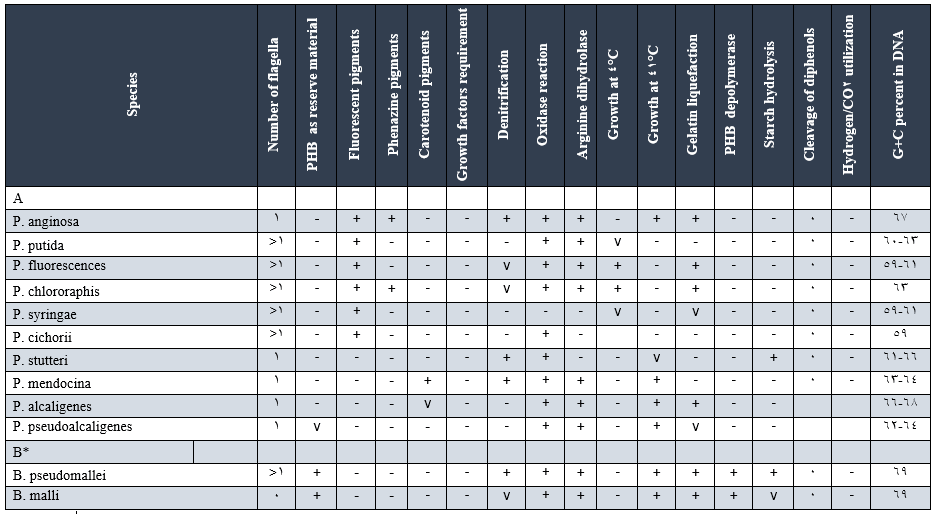
جدول(1): خصوصیات و ویژگیهای بیوشیمیایی سودوموناسها و بورخولدریاها
سروتایپینگ
آنتیژن LPS در سودوموناس، مقاوم به حرارت، اختصاصی گروه بوده که بوسیله تست آگلوتیناسیون بر اساس آنتیژن نوع O سروتیپ میگردد. 90% سوشها دارای این آنتیژن هستند. بر اساس آنتیژن Hء، 50% سوشها دارای این آنتیژن هستند. این آنتیژنها با روشهای ایمونوفلورسنس هم قابل اندازهگیریاند.
باكتریوسین تایپینگ
بر اساس تولید پیوسین صورت میگیرد و یک روش معمول و رایج است، حتی از روش سروتیپ كارآیی بیشتری دارد و برای كلنیهای موكوئیدی هم قابل اجرا است.
درمان
درمان عفونتهای ناشی از سودوموناس آئروژینوزا مشکل است، زیرا که این باکتری بهطور معمول به داروهای متعددی مقاوم است و همچنین برخی از سویهها سفالوسپورینازها را تولید میکنند که میتوانند سفالوسپورینهای نسل سوم را تجزیه کنند، لذا به درمان ترکیبی و یک عامل بتالاکتام ضد سودوموناسی نیاز است. ارگانیسمهای حساس ممکن است در طی درمان آنتیبیوتیکی با تولید آنزیمهای خنثیکننده فعالیت آنتیبیوتیک و یا با انتقال پلاسمیدهای مقاومت از سویههای حساس و یا با موتاسیون در ژن کدکننده پورینهای منافذ غشای خارجی مقاوم شوند. انتقال ایمونوگلوبولین و گرانولوسیت بهمنظور بهبود سیستم ایمنی میتواند در بیماران مبتلا به عفونت سودوموناسی و دارای نقص ایمنی مفید واقع شود. برای درمان معمولاً یکی از انواع پنیسیلینهای فعال علیه سودوموناس نظیر تیکارسیلین یا پیپراسیلین همراه با یک آمینوگلیکوزید نظیر توبرامایسین تجویز میگردد. کینولونها و کارباپنمها دو نوع از آنتیبیوتیکهای جدید با فعالیت ضد سودوموناسی هستند. سیپروفلوکساسین مثالی از یک کینولون با فعالیت خوب ضد سودوموناسی است. در موارد سوختگی، کاربرد موضعی کرم سولفامایلون، کرم سیلور سولفادیازین و یا محلول شستشوی نیترات نقره پذیرفتهشدهترین شکل درمان است. در بیماران سرطانی، درمان ایمونولوژیک در شکل گاماگلوبولین هیپرایمیون و ترانسفورماسیون گرانولوسیت با موفقیت همراه بوده است. سفتازیدیم در درمان اولیه عفونتهای سودوموناس آئروژینوزا بهکار میرود.
آنتیبیوگرام
بطور کلی این باکتریها نسبت به اکثر آنتیبیوتیکها مقاوم هستند و بنابراین لازم است آنتیبیوگرام برای همه سویهها صورت بگیرد. همچنین بررسی الگوی مقاومت دارویی میتواند در تأیید تشخیص مؤثر باشد. سودوموناس آئرژینوزا بجز آمینوگلیکوزیدها، کربوکسی پنیسیلینها و یوریدوپنیسیلینها، سفتازیدیم، سفیپیم، کارباپنمها، کینولونها، کلیستین و پلیمیکسین B به بیشتر داروها مقاومت دارند. البته برخی از انواع این باسیل که از خلط افراد مبتلا به فیبروزیس سیستیک جدا میشوند، حساسیت بیشتری داشته و به آمپیسیلین و نالیدیکسیک اسید حساس هستند. سودوموناس آئروژینوزا همیشه به سولفومتوکسازول–تری متوپریم و تتراسایکلینهای وسیعالطیف مانند تایجیسیکلین، ارتاپنم و نیتروفورانتوئین مقاوماند. مقاومت به چندین دارو در سویههای سودوموناس آئروژینوزا در حال افزایش است، بهخصوص در بخشهای مراقبتهای ویژه و در میان بیماران دارای عفونت طولانی مدت سودوموناس نظیر سیستیک فیبروزیس و سایر سندرومهای مزمن. هنگام مواجهه با ایزولههای مقاوم، از آزمایشگاه خواسته میشود که آنتیبیوتیکهای بیشتری مانند کلیستین یا پلیمیکسین B را تست کنند.
کنترل و پیشگیری
کوشش برای ریشهکنی سودوموناسها از بیمارستانها بیفایده است. استفاده بیرویه آنتیبیوتیکها نیز باید کنترل شود تا مانع از بین رفتن فلور نرمال و ایجاد سویههای مقاوم به آنتیبیوتیک شود. پیشگیری مشکل است، اما با کنترل بهداشتی و دقیق هوادهندهها و فیلترها در واحدهای احتراق، استریلیزاسیون تجهیزات تنفسی درمانی و سرانجام در برخی افراد حساس با واکسیناسیون امکانپذیر است. واکسنهایی که از فرآورده خالصشدهتر به همراه اگزوتوکسین ضعیفشده یا توکسوئید A هستند، مقادیر بیشتری از آنتیبادی را برای مدتهای طولانیتر تحریک میکنند. برخی از محققین واکسنهایی را تکمیل کردهاند که با استفاده از پروتئین F غشای خارجی، فلاژله و یا گلیکوکالیس سودوموناس بوده است. برخی دیگر اعتقاد دارند که بجای واکسینه کردن بیماران به عفونتهای سودوموناسی، بهتر است از ایمونیزاسیون غیرفعال استفاده شود.
در مورد باکتری سودوموناس آئروژینوزا مانند باکتری کزاز میتوان سم آن را جدا و غیرفعال کرد تا از آن در درمان استفاده شود. واکسنی به این منظور ساخته شده است، بنابراین سم این باکتری را جدا و غیرفعال کرده و از خاصیت ایمنیزایی آن میتوان بهره برد. سم ضعیفشده از اگزوتوکسین A از سوشهای سمزای سودوموناس آئروژینوزا تهیه شد و ثابت شد که از این واکسن میتوان در جلوگیری از مرگ افراد در شغلهای پرخطری که دچار سوختگی میشوند استفاده کرد.
با توجه به اینکه سودوموناس آئروژینوزا، آنتیژنهای سطحی و محصولات خارج سلولی فراوانی تولید میکند، امروزه کاندیداهای مختلفی در مورد واکسنهای آن مطرح هستند:
- LPS کونژوگهشده با اگزوتوکسین A باکتری یا با توکسوئید تتانوس
- آلژینات به همراه پلیساکارید با وزن مولکولی بالا و اگزوتوکسین A
- DNA واکسنها (فلاژلین B، اگزوتوکسین A و OmpF)
- افکتورهای تیپ III ترشحی مانند PcrV
بورخولدریا
گونههای بورخولدریا (قبلاً به آن سودوموناس میگفتند) باسیلهای گرم منفی بدون اسپور و هوازی هستند و به استثنای بورخولدریا مالئی همگی متحرک هستند زیرا دارای فلاژل قطبی هستند. این ارگانیسمها کاتالاز مثبت بوده و اکثر آنها اکسیدار مثبتاند. بر روی محیط مک کانگی آگار تولید کلنیهای لاکتوز منفی میکنند. این باکتریها در محیط، آب، خاک و بر روی گیاهان یافت میگردند. به دلیل تمایل آنها به محیطهای مرطوب مانند سودوموناسها در محیط بیمارستان یافت شده و بهطور بالقوه عامل عفونتهای اکتسابی از بیمارستان هستند. دو پاتوژن مهم انسانی در این جنس بورخولدریا سودومالئی و کمپلکس بورخولدریا سپاشیا هستند.
بورخولدریا (سودوموناس) سودومالئی
بورخولدریا (سودوموناس) سودومالئی یا باسیل ویت موریس یک باكتری آزادزی است كه در آبهای گرم و خاک مرطوب جنوب شرقی آسیا یافت میشود. این باكتری در مزارع برنج عامل بیماری بنام ملیوئیدوزیس یا بیماری بمب ویتنام است. عفونت انسانی با بورخولدریا سودومالئی معمولاً با ورود باكتری از طریق زخمها، بریدگیها یا خراشها آغاز میشود، بههرحال در بعضی از موارد، آلودگی از طریق تنفس باكتری توسط فرد سالم یا در افراد بستری در بیمارستان از طریق وسایل برونكوسكوپی و كاتتر ادراری آلوده و یا كاركنان آزمایشگاه در حین كشت بورخولدریا سودومالئی آغاز میشود.
بورخولدریا سودومالئی در گروه rRNA II سودوموناسیه (گروه سودومالئی) قرار دارد. در بیشتر محیطهای كشت استاندارد میكروبیولوژی ایجاد كلنیهای فشرده یا چروکیده شکل میکند. بورخولدریا سودومالئی رنگ را بهصورت دوقطبی به خود گرفته و در زیر میكروسكوپ به شكل سنجاققفلی (Safety pin) دیده میشود. باكتری اكسیداز مثبت است و نیترات را به نیتریت احیا مینماید. لیزین دکربوکسیلاز مثبت و Dnase منفی و به پلیمیکسین مقاوم است. در محیط تریپل شوگرآیرون آگار (TSI) بعد از 24 ساعت بهصورت ایجاد اسید در سطح و خنثی در ته لوله درمیآید ولی بعد از 72 ساعت ته لوله نیز بهصورت اسیدی درمیآید (جدول 1). آنتیسرمها نیز در تشخیص سویههای بورخولدریا سودومالئی استفاده میشوند.
بورخولدریا سپاشیا
این باکتری یک پاتوژن بیمارستانی است که با تجهیزات آلوده، داروها و ضدعفونیکنندهها مرتبط است و میتواند سبب باکتریمی، عفونت دستگاه ادراری، آرتریت عفونی و عفونت دستگاه تنفسی شود. یک پاتوژن مهم در بیماران سیستیک فیبروزیس و در بیماران مبتلا به گرانولوماتوز مزمن است. بیماران مبتلا به سیستیک فیبروزیس که بهطور مزمن با این ارگانیسم آلوده هستند شانس کمی برای زنده ماندن دارند. کمپلکس بورخولدریا سپاشیا حداقل شامل 9 گونه است و همه گونهها از بیماران سیستیک فیبروزیس جداسازی شدهاند، با این حال در ایالات متحده آمریکا تقریباً 85 درصد سویههای بورخولدریا مولتی ورانس و بورخولدریا سنوسپاشیا هستند. بسیاری از مطالعات نشان دادهاند که بورخولدریا سنوسپاشیا دارای فاکتورهای ویرولانس ذاتی است که منجر به افزایش میزان مرگ و میر در بیماران سیستیک فیبروزیس که با این باکتری آلوده شدهاند در مقایسه با سایر سویهها بورخولدریا میگردد.
گونههای بورخولدریا بهخوبی بر روی محیطهای استاندارد آزمایشگاهی شامل ژلوز خوندار و شکلاتی رشد میکنند. جداسازی ایزولههای بورخولدریا سپاشیا از نمونههای آلوده مثل خلط ممکن است از طریق استفاده از محیطهای انتخابی مانند PC (بورخولدریا سپاشیا آگار انتخابی)، محیط OFLP (پلیمیکسین B با پاسخ اکسیداتیو تخمیری، باسیتراسین لاکتوز آگار) و BCSA (بورخولدریا سپاشیا آگار انتخابی) تسهیل گردد. برای مشاهده کلنیهای این باکتریها 3 روز وقت لازم است. بورخولدریا سپاشیا اکسیداز مثبت و لیزین دکربوکسیلاز مثبت است و از گلوکز اسید تولید میکند. لازم به ذکر است که روشهای بیوشیمیایی مناسبی برای افتراق میان کمپلکس بورخولدریا سپاشیا یا بین این کمپلکس و گونههای مرتبط نظیر بورخولدریا گلادیولی، رالستونیا، کوپریاویدوس و گونههای پاندورا وجود ندارد. روشهای مولکولی اغلب جهت تأیید شناسایی نیاز است و هنگامی که شک به کمپلکس بورخولدریا سپاشیا وجود دارد، انجام این روشها توصیه میشود. استفاده از MALDI-TOF نیز ممکن است در آینده منجر به شناسایی گونههای جدید گردد.

بورخولدریا سپاشیا به بسیاری از عوامل ضدمیکروبی بسیار مقاوم است، اما معمولاً به پیپراسیلین، سفتازیدیم، کلرامفینکل و تریمتوپریم–سولفومتوکسازول حساس است. سویههای جداشده از بیماران سیستیک فیبروزیس که تحت درمان آنتیبیوتیکی متعدد قرار میگیرند احتمالاً مقاوم به این عوامل میگردند. CLSI تنها سفتازیدیم، مروپنم، مینوسیکلین و تریمتوپریم–سولفومتوکسازول را برای بورخولدریا سپاشیا توصیه کرده است. همه ارگانیسمهای بورخولدریا سپاشیا بهصورت ذاتی به پلیمیکسینها (کلیستین) مقاوم هستند.






یک دیدگاه