اصول و روشهای نشان دادن قارچها در نمونههای کلینیکی – آزمایش مستقیم و کشت (بخش دوم)
ترجمه و تنظیم: دکتر محمد قهری
4-3- سایر ملاحظات ایمنی زیستی
موارد زیر بعنوان احتیاطات استاندارد در ارتباط با کار کردن با کپکهایی که از نمونههای بیومدیکال جدا میشوند باید در نظر گرفته شوند:
• هیچوقت نباید درب پلیت های حاوی کشت کپک ها خارج از هود بیولوژیک (BSC) باز شوند.
• به منظور اجتناب از استنشاق ارگانیسمهای بالقوه خطرناک، بو کردن یا بوکشیدن (sniffing) کشتها نباید انجام شود.
• برای آماده کردن کپکها برای انجام آزمایشهای میکروسکوپی بهترین کار این است که از مایعات مونت کنندهای استفاده شود که قارچها را در حالت غیرزنده نگاه میدارد (بعنوان مثال میتوان از رنگهای واجد فنل استفاده کرد).
• یک ظرف ثانویهی مناسب (محافظ) برای انتقال کشت های قارچی در داخل فضای آزمایشگاه باید بکار رود. در نتیجه هر گونه سقوط تصادفی یا حادثهی شکستن بصورت لوکالیزه باقی مانده و امکان گسترش به قسمتهای مختلف آزمایشگاه نخواهد بود.
• به منظور نگهداری قارچها برای مدتهای طولانی، میتوان از روشهایی مثل تهیهی سوسپانسیونی از اسپورها در آب استریل و نگهداری در دمای اتاق، یا سوسپانسیون اسپورها در گلیسرول استریل 10% تا 20 درصد که در فریزرهای با سرمای زیاد و یا در نیتروژن مایع نگهداری میشوند، استفاده نمود.
• توصیه میشود برای کپکهای بالقوه خطرناک از ظروف نگهداری انفرادی استفاده شود و با علامت مناسبی پتانسیل خطر افزایش یافته را نشان داد.
• نواحی نگهداری باید به کمک برچسبهای ایمنی زیستی مناسب شناسایی شوند و دسترسی به این مناطق فقط به افراد مجاز (authorized) محدود گردد (بعنوان مثال برچسبی شبیه به تصویر زیر).

• حمل و نقل نمونهها به خارج از آزمایشگاه باید مطابق با مقررات و قوانین مراکز معتبر بینالمللی، ملی، و محلی انجام گیرد.
• این دستورالعملها نیازمندیهای اختصاصی را برای بستهبندی و برچسب گذاری فراهم میکنند.
• از حمل و نقل و جابجایی پلیتهای تلقیح شده اجتناب شود و در صورت امکان کشتها را در شرایط تلقیح شده در لوله انتقال دهید.
4-4- پرسنل
پایه و اساس یک آزمایشگاه ایمن، تربیت مناسب کارمندان جدید و برگزاری کلاسهای یادآوری بصورت منظم برای تمام کارمندان است. دستورالعملهای ایمنی زیستی باید مکتوب شده و بصورت روزمره در آزمایشگاه عادت شده و بصورت رسم و روال منظم درآیند. فقط آن دسته از پرسنلی که بقدر کافی تربیت شده و شایسته و لایق و کارآمد تشخیص داده شدهاند میتوانند در آزمایشگاه مشغول به کار باشند. شایسته و بایسته است که پرسنل آزمایشگاه در مورد عناصر اساسی پاتوژنز قارچها، فاکتورهای خطر، و راههای کنترل آموزش داده شوند. اوضاع زمینهای (مانند وضعیتهای مستعد کنندهی ایمنی، فاکتورهای ژنتیکی، و حاملگی) که میتوانند افزایش حساسیت به عفونتهای مهاجم قارچی را مطرح کنند نیز مورد بحث و آموزش قرار گیرند. لازم است نمایش آشکار تجهیزات حفاظتی پرسنل در تمام نواحی کاری وجود داشته باشد و به این وسیله یک یادآور ثابت برای کارمندان فراهم شده و نیز بازرسیهای دورهای مورد تاکید قرار گیرد.
یک سیاست و روش گزارش حوادث برای مدیریت هرگونه تخلف و شکست در شیوههای کار آزمایشگاهی بکار گرفته شود و مواد ریخته شده یا رها شدهی اتفاقی مورد رسیدگی قرار گیرد.
هرگونه مواجههی اتفاقی با قارچهای خطرناک باید با شتاب و به سرعت به کمک دستورالعملهای مواجههی شغلی و ایمنی زیستی سازمانی که قبلا تهیه و تمرین شده است مدیریت شود.
مسئول آزمایشگاه و سوپروایزر باید به طور نزدیک با افسر ایمنی زیستی سازمانی کار کنند و متخصصین ایمنی زیستی فعالیت خود را برای اطمینان حاصل کردن از یک محیط ایمن کاری برای پرسنل آزمایشگاه متمرکز کنند.
5- سطوح آزمایشگاه و خدمات ارجاعی
تصمیم اینکه خدمات آزمایشگاه قارچشناسی تشخیصی تا چه سطحی فراهم شود، تصمیمی است که یک موسسه باید بر اساس جمعیت بیماران، تعداد کارمندان و سطح علمی و مهارتی آنان، امکانات و وسایل، و حجم آزمایشات قارچ شناسی بگیرند. بسیاری از بیمارستانها و کلینیکهای کوچکتر به راحتی میتوانند خدمات پایهای برای کشت قارچها فراهم کنند اما همانطور که در بخش 4/2 بحث شد ممکن است نیاز به ارجاع کشت و ارگانیسمهای زنده به بیمارستانهای بزرگتر یا آزمایشگاه رفرانس داشته باشند که در آنجا اقدامات بعدی بر روی کشتها بعمل میآید.
آزمایشگاههای بیمارستانی متوسط ممکن است امکاناتی برای کشت مجدد و عملیات شناسایی قارچها داشته باشند و ممکن است لیستی از تستهای اختصاصی برای شناسایی مخمرهای شایع (مثلا گونههای کاندیدا) و یا کپکهای انتخاب شدهای مثل گونههای آسپرجیلوس و غیره فراهم کرده باشند.
اگر پرسنل آزمایشگاههای متوسط بیمارستانی تجربه یا تخصص و مهارت لازم جهت فراهم کردن سرویسهای شناسایی برای طیف وسیعی از قارچها را نداشته باشند، در اینصورت شناسایی ارگانیسمهایی بغیر از جنسها و گونههای شایعتر اغلب به ازمایشگاههای رفرانس یا به آزمایشگاههای بزرگتر ارجاع میشوند. بیمارستانهای بزرگ و آزمایشگاههای رفرانس اغلب دارای این توانایی هستند که طیف کاملی از روشهای شناسایی قارچها را فراهم کرده باشند که شامل تکنیکهای ملکولار مانند پروبهای هیبریدیزاسیون اسیدهای نوکلئیک برای قارچهای دیمورفیک و PCR برای شناسایی براساس توالی اسیدهای نوکلئیک خواهد بود.
علاوهبر این، این آزمایشگاهها میتوانند تستهای تعیین حساسیت برای مخمرها و در برخی موارد برای کپکها را فراهم کنند. منابع چاپ شدهای وجود دارند که چگونگی انتخاب یک آزمایشگاه رفرانس را راهنمایی میکنند. برنامههای تستهای مهارتی در ایالات متحده آمریکا از طریق منابع مختلف قابل فراهم است. این منابع در پایگاه اینترنتی مرکز خدمات مراقبت و کمکهای پزشکی لیست شده است:
http://www.cms.gov/regulations-and-guidance/legislation/CLIA/downloads/ptlist.pdf
منابع دیگر شامل ارزیابی کیفیت خارجی بریتانیای کبیر (http://www.ukneqas.org.uk)، برنامهی مدیریت کیفیت خدمات آزمایشگاهی در انتاریو، کانادا (http://www.qmpls.org) و برنامههای تضمین کیفیت کالج سلطنتی پاتولوژیستهای استرالیا در استرالیا و آسیای جنوب شرقی (http://www.rcpaqap.com) هستند.
برنامههای تست مهارتی (انجام آزمایش روی نمونههای کنترل کیفی خارجی) شناسایی مخمر و کپک، تستهای حساسیت داروهای ضد قارچی، و تست آنتی ژن کریپتوکوکال را مورد بررسی (بازبینی و ارزیابی) قرار میدهند. آزمایشگاهها باید همان پروتکلهای تست و آزمایشات را به همان صورتی که برای نمونههای بیماران انجام میدهند برای نمونههای تستهای مهارتی نیز انجام دهند و نیز آگاه باشند که نمونههای تستهای مهارتی نباید برای شناسایی به آزمایشگاه دیگر ارجاع شوند (به سند GP26 استاندارد CLSI مراجعه شود).
6- کنترل کیفیت و نگهداری کشتهای ذخیره
6-1- کنترل کیفیت محیطهای کشت و مواد و معرفها
توصیه میشود که تمام محیطهای کشت، معرفها، وسایل پلاستیکی و سایر موادی که در آزمایش بکار گرفته میشوند از کیفیت بالا برخوردار باشند و اسناد کیفیت آنها از فروشنده خواسته شود. هنگامیکه منابع خارجی (نظیر مواد و معرفها) استفاده میشود اطلاعات مربوط به نام محصول، دادههای مربوط به تولید (مانند ترکیب، شماره سری تولید یا batch number و تاریخ انقضاء) باید ثبت شوند. منابعی که فاقد این اطلاعات هستند و یا در محیط بدون سیستم مدیریت کیفیت (QMS) تولید شدهاند عموما نباید برای کارهایی که در این سند شرح داده شده است بکار گرفته شوند.
6-2- کنترل کیفیت استرین های رفرانس
استرینهای رفرانس QC نوعا توسط متخصصین انتخاب میشوند و معمولا بعد از غربالگری تعداد زیادی استرینهای مرتبط با یکدیگر که در خواص مورد نظر اشتراک دارند (مثلا درجهی بالایی از پایداری خصوصیات فنوتیپیک و ژنوتیپیک دارند و آستانهی غلظت حساسیت یا مقاومت به یک مادهی شیمیایی در آنها بسیار نزدیک به یکدیگر است) انتخاب میشوند. هنگامیکه استرینهای رفرانس QC برای یک روش یا فرآیند خاصی انتخاب شدند نوعا در یک مرکز دارای تجهیزات خوب و معتبر میکروبی به منظور حفاظت ایمن و طولانی مدت نگهداری میشوند. از جملهی این گونه مراکز میتوان کلکسیون آمریکایی کشت میکروارگانیسمها، و مرکز تنوع زیستی آکادمی سلطنتی علوم و هنر هلند را نام برد. مرکز فراهم کننده (تهیه کننده) استرین رفرانس باید توانایی نگهداری میکروارگانیسمها را درطول چندین دهه با حداقل میزان آلودگی داشته باشند و این کشتها را برای استفاده در آزمایشگاههای مختلف تولید کنند. بسیاری از تامین کنندگان استرینهای رفرانس دارای سیستم مدیریت کیفیت مطلوب و گواهینامههای موسسات مربوطه بر طبق استانداردهای ISO میباشند.
6-2-1- نگهداری استرین های رفرانس
در یک آزمایشگاه میکروب شناسی پزشکی، استرینهای رفرانس بعد از تهیه باید برای کاهش پتانسیل تغییرات فنوتیپیک و ژنوتیپیک با حداقل پاساژ نگهداری شوند (به سند M22 استاندارد CLSI رجوع شود). کشتهای ذخیرهی استرینهای رفرانس بوسیلهی تلقیح سلولها بطور مستقیم از ظرف اصلی خریداری شده به داخل محیطهای کشت مناسب تهیه میشوند. سلولها از کشتهای فعال در حال رشد برداشت شده و در یک محلول مقاوم در مقابل انجماد (cryoprotectant) نظیر گلیسرول 10 تا 15 درصد سوسپانسیون میشوند. روش دیگری که در آن از دانههای متخلخل استفاده میشود نیز قابل بهرهبرداری است. این ماده باید به صورت فریز شده در ازت مایع و یا در فریزر با برودت بسیار پائین (کمتر از منفی 70 درجهی سانتیگراد) نگهداری شوند. برخی از قارچها ممکن است در شرایط انجماد بخوبی بقیه زنده نمانند. ویالهای منجمد میتوانند به عنوان کشتهای ذخیره نگهداری شوند و از آنها کشتهای مورد نیاز را تهیه کرد.
روشهای دیگر برای نگهداری با دورهی کوتاهتر (یعنی 1 تا 5 سال) برای ایزولههای ذخیره فراهم هستند. در بین این روشها روش کشت در آب بدلیل سادگی و سودمندی، از ارزش خوبی برخوردار است. در این روش سلولهای مخمری، کنیدیها و یا هایفیها در حجم 2 الی 3 میلیلیتر آب استریل و دیونیزه در یک ظرف نفوذناپذیر (leak-proof) سوسپانسیون شده و در دمای اتاق نگهداری میشوند. برای تهیهی یک کشت تازه، با انتقال یک قطره از این سوسپانسیون به محیط کشت مناسب اقدام میگردد. (به سند M22 استاندارد CLSI رجوع شود).
6-2-2- استفاده و بهره برداری کردن از استرینهای رفرانس
6-2-2-1- برنامه ی انتقال
برنامه یا جدول زمانی برای انتقال میتواند برای آمادهسازی ارگانیسمهای QC مورد استفاده قرار گیرد. (به سند M22 استاندارد CLSI رجوع شود).
1- کنترل استوک
حداقل سالی 2 مرتبه از هر ارگانیسم QC که به صورت روتین در آزمایشگاه استفاده میشود، یک کشت تهیه کنید. هنگامیکه یک ویال از استرین رفرانس استوک را از درون تانک ازت مایع یا فریزر 70- درجهی سانتیگراد بر میدارید برای اجتناب از ذوب شدن، آن را در یخ خشک نگاه دارید. بخشی از ارگانیسم رفرانس را بوسیلهی شکستن چند کریستال یخ از سطح ویال بردارید و یا یک دانه (bead) را برداشته و به سطح پلیت یا لولهی آگار سابورو گلوکز آگار (ترجیحا برای مخمرها و برای کپکها ترجیحا از محیط PDA استفاده شود) تلقیح کنید. سپس فورا ویال استوک رفرانس را به تانک ازت مایع یا فریزر 70- درجه سانتیگراد برگردانید. لوله یا پلیت را به عنوان کنترل استوک برچسب بزنید و نام ارگانیسم و تاریخ تلقیح در آن ثبت شود. سپس آن را در دمای 2± 30 درجهی سانتیگراد به مدت 2 الی 3 روز انکوبه نمائید یا اینکه تا زمانیکه رشد خوبی بدست آید. سپس دور درب پلیت را بخوبی سیل کنید و در دمای 2 الی 8 درجه سانتیگراد نگهداری نمائید. به عنوان یک راه دیگر قارچهایی که به صورت منجمد و یا در آب نگهداری میشوند میتوان از آنها بعنوان کنترل استوک استفاده کرد.
2- کنترل کاری
از کنترل استوک یک کشت مجدد تهیه کنید. روی ظرف مربوطه برچسبی بزنید که روی آن نام کنترل کار، نام ارگانیسم و تاریخ تلقیح ثبت شود. به مدت 2 تا 3 روز انکوبه نمائید یا تا زمانی که رشد خوبی بدست آید. این نمونه را در دمای 2 الی 8 درجه سانتیگراد برای حداکثر 4 هفته نگهداری کنید. حداقل یکبار در ماه با استفاده از کنترل ذخیره که که در یخچال نگهداری میکنید یا از کشت آب و یا از کنترل ذخیرهی فریز شده، یک کنترل کاری تازه تهیه نمائید.
هر موقع که کنترل کاری کهنه شده و در خواص فنوتیپیک و ژنوتیپیک آن نسبت به خصوصیات تعریف شده اختلاف و انحرافی (deviation) رخ دهد باید یک کنترل کاری جدید تهیه شود. هنگامیکه کشت را انتقال میدهید هرگز فقط یک کلنی منفرد را انتخاب نکنید و بجای آن حداقل 5 کلنی انتخاب کنید تا نمونهای که نمایندهی ژنوتیپیک باشد فراهم گردد. هنگامیکه یک کشت رفرانس مورد استفاده قرار میگیرد چک کردن خلوص آن بسیار اهمیت دارد. پرسنل آزمایشگاه باید با ویژگیهای پایهای ارگانیسمهای کنترل کیفی مورد استفاده آشنا باشند (به عنوان مثال با مرفولوژی ماکروسکوپی و میکروسکپی آن).
6-2-2-2- آزمایش کنترل کیفیت محیط ها و معرف ها
برطبق سند M22 استاندارد CLSI از یک کشت در حال رشد فعال که از کنترل کاری تهیه کردهاید نمونهی تلقیح (اینوکولوم) را بردارید. مقدار زمانی که برای بدست آوردن یک کشت در حال رشد فعال مورد نیاز است بستگی به نوع ارگانیسم دارد (مثلا برای مخمرها 24 تا 48 ساعت، برای گونههای کریپتوکوکوس تا 72 ساعت و کپکها چندین روز تا چندین هفته است).
رنگها را میتوان مستقیما با این کشت تست کرد. به محیطهای کشت میتوان به طور مستقیم تلقیح کرد و یا از طریق تهیهی یک کشت تلقیح شدهی استاندارد شده، این کار را انجام داد. مورد اخیر امکان بررسی قابلیت تکرار را برای ارزیابی رشد و خواص مهار کنندگی بیشتر نشان میدهد و انجام آن عالیتر است. تلقیح سبکتر برای ارزیابی خواص مواد مغذی محیط کشت مناسبتر و تلقیح سنگینتر برای ارزیابی خواص مهار کنندگی آن مناسبتر است. یک تلقیح استاندارد شده به وسیلهی رقیق کردن کشت فعال در سالین مطابق با استاندارد 0/5 مک فارلند بدست میآید.
- برای محیطهای کشت غیرانتخابی، سوسپانسیون با رقت 1/100 یا 1/1000 تهیه کنید. هدف بدست آوردن رشد کافی با مرفولوژی تایپیکال است، هنگامیکه 10 میکرولیتر از سوسپانسیون برروی محیط کشت تلقیح شده باشد.
- برای محیطهای کشت انتخابی، سوسپانسیون را با رقت 1/10 یا 1/100 تهیه کنید و مطابق بالا عمل نمائید.
- برای محیطهای کشتی که در لوله تهیه میشوند مقدار 10 میکرولیتر از سوسپانسیون 0/5 مک فارلند رقیق نشده را تلقیح کنید. مقدار تلقیح را مطابق با نیاز به رشد سبکتر یا سنگینتر تنظیم کنید.
محیطهای کشت را بر طبق روشهای روتین انکوبه کنید و برای رشد کافی و مرفولوژی تایپیکال مورد آزمایش قرار دهید و نیز در صورت استفاده از محیط انتخابی برای مهار رشد بررسی کنید.
6-2-3- تعداد دفعات تست کنترل کیفی
رفرانسهایی در دسترس هستند که دستورالعمل تعداد تستهای کنترل کیفی را بر طبق روش تست یا محیط کشت و یا رنگهایی که بکار گرفته میشوند فراهم میکنند (به سند M22 استاندارد CLSI رجوع شود). اگرچه فراوانی تستهای کنترل کیفی بر طبق نظر آژانسهای وابسته به نظارت و اعتبار بخشی ممکن است با یکدیگر تفاوت داشته باشند و انواع معینی از محیطهای کشت تجارتی ممکن است معاف و مستثنی شوند. جداول شماره 2 و 3 دستورالعملهای مطرح شده برای محیطهای کشت و رنگآمیزیهای قارچشناسی را لیست کرده است. بهطور کلی یک یا دو واحدی که بهطور اتفاقی از هر batch از محیطهای کشت، معرفها، و غیره انتخاب میشوند باید با استفاده از استرینهای کنترل کیفی یا رفرانس مورد آزمایش قرار گیرند.

| جدول2- استانداردهای اجرایی کنترل کیفی برای محیطهای کشت قارچی | |||
| محیط کشت | ارگانیسمهای پیشنهادی QCء (CLSI-M22) | انکوباسیون | نتایج مورد انتظار |
| BHI با یا بدون 5% خون گوسفند با جنتامایسین و یا کلرامفنیکل pH 7.4 | کاندیدا آلبیکنس
آسپرجیلوس برازیلینسیس آسپرجیلوس فومیگاتوس تریکوفیتون منتاگروفایتیس نوکاردیا آستروئیدس اشریشیا کولی |
30±20C
بمدت 1 تا 3 روز |
رشد (مخمری سفید)
رشد (کلنی سفید کنیدیهای سیاه) رشد (کلنی آبی سبز) رشد رشد عدم رشد |
| آگار کروموژنیک (گونههای کاندیدا) | کاندیدا آلبیکنس
کاندیدا کروزی کاندیدا تروپیکالیس کاندیدا گلابراتا سودوموناس آئروژینوزا |
35±20C
بمدت 2 تا 3 روز |
برای رنگ کلنی به روشهای QC شرکت سازنده مراجعه شود.
عدم رشد |
| سابورو با جنتامایسین و کلرامفنیکل pH 6.7 | کاندیدا آلبیکنس
آسپرجیلوس برازیلینسیس تریکوفیتون منتاگروفایتیس اشریشیا کولی |
30±20C
بمدت 1 تا 3 روز |
رشد
رشد رشد عدم رشد |
| Potato Dextrose Agar | کاندیدا آلبیکنس
تریکوفیتون منتاگروفایتیس تریکوفیتون روبروم |
30±20C
بمدت 1 تا 3 روز |
رشد رشد،کلنی کرم رنگ و سفید. عدم پیگمان در پشت کلنی رشد،کلنی سفید. تولید پیگمان قرمز شرابی در پشت کلنی |
| سابورودکستروز آگار (امونس) pH 6.9 | کاندیدا آلبیکنس
آسپرجیلوس برازیلینسیس تریکوفیتون منتاگروفایتیس |
30±20C
بمدت 1 تا 3 روز |
رشد
رشد رشد |
| سابورودکستروز آگار (امونس) با کلرامفنیکل pH 6.9 | کاندیدا آلبیکنس
آسپرجیلوس برازیلینسیس تریکوفیتون منتاگروفایتیس اشریشیا کولی |
30±20C
بمدت 1 تا 3 روز |
رشد
رشد رشد عدم رشد |
| سابورودکستروز آگار (امونس) با کلرامفنیکل و سیکلوهگزامید (یا: مایکوبیوتیک آگار و یا: مایکوزیل آگار) | کاندیدا آلبیکنس
آسپرجیلوس برازیلینسیس تریکوفیتون منتاگروفایتیس ساکارومیسس سرویسیه اشریشیا کولی |
30±20C
بمدت 1 تا 3 روز |
رشد
مهار نسبی رشد خوب عدم رشد عدم رشد |
| کورن میل آگار تووین 80 | کاندیدا آلبیکنس | 26-280C | رشد سودوهایفی، بلاستوکونیدی، و وزیکولهای با دیواره ضخیم انتهایی (کلامیدوکونیدی) |
| مالت اکسترکت آگار | تریکوفیتون منتاگروفایتیس
اشریشیا کولی |
26-280C | رشد کلنی سفید
عدم رشد |
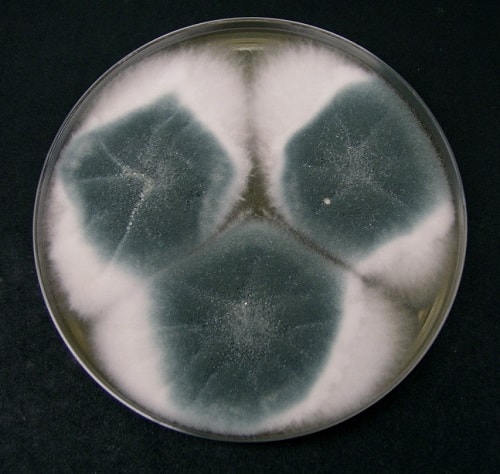
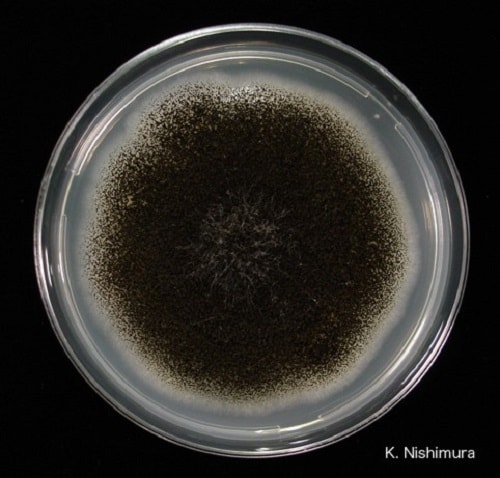
| چاپک دوکس آگار | آسپرجیلوس برازیلینسیس
آسپرجیلوس فومیگاتوس |
26-300C | رشد (کلنی سفید کنیدیهای سیاه)
رشد (کلنی آبی سبز) |
| Birdseed Agar | کاندیدا آلبیکنس
کریپتوکوکوس نئوفرمنس واریته نئوفرمنس |
26-300C | رشد کلنیهای سفید
رشد کلنیهای قهوهای رنگ |
| محیط کشت برنج
(Rice grain medium) |
میکروسپوروم کنیس | 26-280C | رشد، میسلیومهای هوائی سفید رنگ (میکروسکوپی: تولید فراوان ماکروکونیدی دوکی شکل با زائده پستانکی) |
| جدول3- استانداردهای اجرایی QC برای رنگ آمیزیهای معمولی مورد استفاده در آزمایشات مستقیم میکروسکپی قارچ شناسی | ||
| رنگ یا معرف | ارگانیسم مناسب برای کنترل کیفی | نتایج مورد انتظار |
| کالکوفلور سفید/پتاس | کاندیدا آلبیکنس
اشریشیا کولی |
فلئورسانس عناصر قارچی
عدم فلئورسانس عناصر قارچی |
| گرم | استافیلوکوکوس اورئوس
اشریشیا کولی |
کوکسیهای گرم مثبت (ارغوانی)
باسیلهای گرم منفی (صورتی) |
| مرکب چین | کریپتوکوکوس نئوفرمنس
کاندیدا آلبیکنس |
سلولهای مخمری با هالهی شفاف و خوب مشخص شده
سلولهای مخمری با هالههای نامنظم یا بدون هاله |
| پتاس | گونههای کاندیدا در نمونهی مثبت پوست یا ناخن | مشاهدهی عناصر قارچی با شفاف شدن بقایای سلولی |