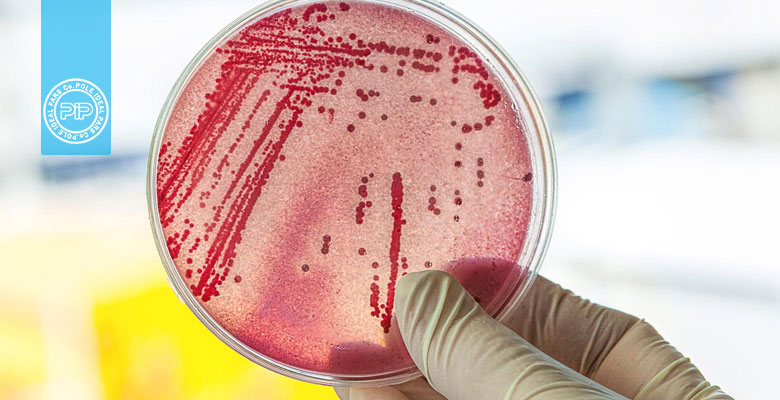
شمارش باکتری اشریشیا کلی و کلی فرمها در مواد غذایی
اشریشیا کلی (Escherichia coli) که در ابتدا با نام کمون باکتریوم کولی (Bacterium coli commune) شناخته میشد، در سال 1885 توسط متخصص اطفال آلمانی به نام تئودور اشریچ (Theodor Escherich) شناسایی شد. اشریشیا کلی به طور گستردهای در روده انسان و حیوانات خونگرم وجود دارد. این باکتری بیهوازی اختیاری در روده و بخشی از فلور اساسی روده است که فیزیولوژی میزبان سالم را حفظ میکند.
باکتری اشریشیا کلی عضوی از خانواده انتروباکتریاسیا (Enterobacteriaceae) است. انتروباکتریاسیا بسیاری از گونههای باکتریایی از جمله عوامل بیماریزای شناخته شدهای مانند سالمونلا، شیگلا و یرسینیا را در بر میگیرند. اگرچه اکثر سویههای اشریشیا کلی به عنوان عوامل بیماریزا در نظر گرفته نمیشوند، اما میتوانند پاتوژنهای فرصت طلب باشند که باعث ایجاد عفونت در میزبانان دارای نقص ایمنی میشوند.
علاوه براین سویههای بیماریزای اشریشیا کلی وجود دارد که در صورت بلع، باعث بیماری دستگاه گوارش در انسانهای سالم میشود.
در این مطلب قصد داریم تا در رابطه با باکتری اشریشیا کلی و نحوه شناسایی آن در مواد غذایی اطلاعاتی ارائه کنیم. پس در ادامه با ما همراه باشید.
۱. مروری بر تاریخچه اشریشیا کلی و مفهوم کلی فرم
در سال 1892 باکتری اشریشیا کلی به عنوان شاخصی برای تعیین این موضوع که آیا آب و مواد غذایی به مدفوع آلوده هستند یا خیر معرفی شد. این امر بر این اساس بود که E. coli در مدفوع انسان و حیوانات به وفور یافت میشود. علاوه بر این، از آنجا که باکتری اشریشیا کلی به راحتی از طریق توانایی تخمیر گلوکز قابل تشخیص است (توانایی تخمیر گلوکز بعدها به توانایی تخمیر لاکتوز تغییر یافت) جداسازی آن از پاتوژنهای شناخته شدهی دستگاه گوارش آسانتر بود.
اگرچه استفاده از اشریشیا کلی به عنوان شاخص آلودگی مدفوع صحیح بود، اما باکتریهای رودهای دیگری مانند سیتروباکتر، کلبسیلا و انتروباکتر نیز وجود داشتند که هم توانایی تخمیر لاکتوز را داشته و هم در خصوصیات فنوتیپی مشابه E. coli بودند. این موضوع استفاده از اشریشیا کلی را به عنوان شاخصی برای تعیین آلودگی آب و مواد غذایی به مدفوع در عمل دشوار و پیچیده میکرد.
در نتیجه، اصطلاح “کلی فرم (coliform)” برای توصیف این گروه از باکتریهای روده ابداع شد. کلیفرم یک طبقه بندی باکتریایی نیست بلکه اصطلاحی است که برای توصیف گروهی از باکتریهای میلهای بیهوازی و گرم منفی مورد استفاده قرار میگیرد که در دمای 35 درجه سانتیگراد و در مدت 48 ساعت قادر به تخمیر لاکتوز و تولید گاز هستند.
اگرچه كلیفرمها به راحتی قابل تشخیص بودند، اما ارتباط آنها با آلودگی مدفوع کمی سوال برانگیز بود زیرا بعضی از كلیفرمها به طور طبیعی در نمونههای محیطی یافت میشوند. این امر منجر به معرفی کلی فرمهای مدفوعی به عنوان شاخص آلودگی شد. کلی فرم مدفوعی زیرمجموعهای از کلی فرمهای کلی هستند که در دمای انکوباسیون بالا، رشد کرده و لاکتوز را تخمیر میکنند. از این رو کلی فرمهای حرارتی نیز نامیده میشوند.
تجزیه و تحلیل کلی فرم مدفوعی برای مواد غذایی در دمای ۴۵/۵ درجه سانتی گراد انجام میشود. اما بررسی آب در دمای ۴۴/۵ درجه سانتیگراد صورت میگیرد.
گروه کلی فرم مدفوع بیشتر از اشریشیا کلی تشکیل شده اما برخی از ارگانیسمهای رودهای دیگر مانند کلبسیلا نیز میتوانند در این دما لاکتوز را تخمیر کنند و بنابراین به عنوان کلی فرم مدفوعی در نظر گرفته میشوند.
۲. شمارش اشریشیا کلی و کلی فرمها برای تعیین آلودگی مواد غذایی و آب
آلودگی آب و مواد غذایی ناشی از مدفوع یک مشکل جدی محسوب میشود. با آزمایش یک ارگانیسم “شاخص” مانند باکتریهای کلی فرم، وجود عوامل بیماری زا با شواهد غیر مستقیم تعیین میشود. آزمایش باکتریهای کلی فرم میتواند نشانه معقولی از وجود سایر باکتریهای بیماریزا در مواد غذایی باشد. در سال 1914 نیز، سرویس بهداشت ایالات متحده شمارش کلی فرمها را به عنوان استانداردی مناسب از نظر بهداشتی پذیرفت.
در حال حاضر، هر 3 گروهِ زیر به عنوان شاخص اما در کاربردهای مختلف مورد استفاده قرار میگیرند.
- کلی فرم
- کلی فرم مدفوعی
- باکتری اشریشیا کلی
تشخیص کلی فرم به عنوان شاخص کیفیت بهداشتی آب یا به عنوان شاخص کلی وضعیت بهداشتی در محیط فرآوری مواد غذایی استفاده میشود.
کلی فرم مدفوعی یک شاخص استاندارد برای آب و صدف دریایی است.
تشخیص باکتری اشریشیا کلی نیز برای نشان دادن آلودگی مدفوعی که به تازگی حین تولید مواد غذایی رخ داده و یا بررسی فرآیند غیر بهداشتی استفاده میشود.
تقریباً تمام روشهایی که برای تشخیص E. coli، کلی فرمهای کلی یا کلی فرمهای مدفوعی استفاده میشود، روشهای شمارشی (enumeration methods) و بر مبنای تخمیر لاکتوز هستند.
روش محتملترین تعداد (MPN) یک روش آماری چند مرحلهای شامل مراحل احتمالی، تأیید شده و تکمیل شده است. در این روش، رقتهای سِریالی یک نمونه در محیط آبگوشت تلقیح میشوند.
۳. روش مرسوم برای شناسایی کلی فرم، کلی فرم مدفوع و E. coli
۱-۳.تجهیزات و مواد لازم
- حمام آب پوشیده شده با سیستم سیرکولاسیون برای حفظ دمای 0.2 ± 44.5 درجه سانتیگراد
- دماسنج غوطه وری با مشخصات: 55-1 درجه سانتیگراد، حدود 55 سانتیمتر، درجهبندی 0.1
- انکوباتور 0.5 ± 35 درجه سانتیگراد
- ترازو با ظرفیت بیشتر از 2 کیلوگرم و حساسیت 0.1 گرم
- همزن آزمایشگاهی
- پیپتهای مدرج 1 و 10 میلی لیتری
- ظروف استریل برای استفاده از نمونه
- بطریهای رقت ساخته شده از شیشه بوروسیلیکات، با درپوش پیچی پلیاتیلن مجهز به عایق تفلون. از بطری های رقت آماده شده تجاری که حاوی بافر فسفات باترفیلد استریل هستند نیز میتوان استفاده کرد.
- کلنی کانتر با لنز بزرگنمایی
- نور ماورا بنفش موج بلند [حدود 365 نانومتر] ، بیش از 6 وات نباشد.
- pH متر
۲-۳. محیط کشت
- محیط کشت آبگوشت سبز درخشان دارای لاکتوز و صفرا 2%
- آبگوشت لوریل تریپتوز
- آبگوشت لاکتوز
- آبگوشت EC
- آگار ائوزین-متیلن بلو
- آبگوشت تریپتون
- آبگوشت MR-VP
- محیط سیترات کوثر
- محیط کشت پلیت کانت آگار
- معرف کواکس
- معرفهای Voges-Proskauer
- معرف رنگ آمیزی گرم
- اندیکاتور متیل قرمز
- لاکتوز صفراوی بنفش قرمز
- آگار VRBA-MUG
- محیط EC-MUG
- محیط کشت تریپتوز لوریل
- رقیق کننده پپتون
۳-۳. آزمایش MPN پیش فرض برای کلی فرم، کلی فرم مدفوع و E. coli
۱. 50 گرم از ماده غذایی را در همزن آزمایشگاهی بریزید. اگر نمونه یخ زده است آن را حدودا 18 ساعت در دمای 2 الی 5 درجه سانتیگراد قرار دهید تا نرم شود. اما دقت داشته باشید کاملا ذوب نشود.
۲. 450 میلی لیتر آب بافر فسفات باترفیلد را به نمونه اضافه کرده و به مدت 2 دقیقه مخلوط کنید.
نکته: اگر نمونه کمتر از 50 گرم بود، نیمی از نمونه را وزن کنید و به اندازه کافی رقیق کننده استریل اضافه کنید تا رقت 1:10 ایجاد شود. حجم کل درون همزن باید به گونهای باشد که تیغههای همزن پوشیده شوند.
۳. رقتهای مختلف نمونه را با استفاده از رقیق کننده فسفات باترفیلد استریل یا معادل آن تهیه کنید. تعداد رقتهای آماده شده بستگی به تراکم کلی فرم پیش بینی شده دارد. تمام سوسپانسیونها را 25 مرتبه با زاویه 30 درجه تکان دهید و یا به مدت 7 ثانیه درون ورتکس میکسر قرار دهید.
۴. حداقل 3 رقت متوالی تهیه کنید. 1 میلی لیتر از هر رقت را درون 3 لوله حاوی LST تلقیح کنید.
۵. از آبگوشت لاکتوز نیز ممکن است استفاده شود.
۶. برای دقت بهتر، از پیپت 1 میلی لیتر یا 5 میلی لیتر برای تلقیح استفاده کنید. حین انتخاب پیپت به حجم نمونه دقت کنید. به عنوان مثال برای برداشتن 0/5 میلیلیتر نمونه از پیپت 10 میلی لیتری استفاده نکنید.
۷. پیپت را به صورت زاویهدار نگه دارید.
۸. از زمان مخلوط شدن نمونه نباید بیشتر از 15 دقیقه بگذرد تا اینکه کلیه رقت ها در محیط مناسب تلقیح شوند.
۹. فاصله زمانی بین مخلوط کردن نمونه تا اینکه کلیه رقتها در محیط مناسب تلقیح شوند نباید بیشتر از 15 دقیقه بطول بکشد.
۱۰. لولههای LST را به مدت ۲±۲۴ ساعت در دمای 0.5 ± 35 درجه سانتیگراد انکوباسیون کنید. سپس لولهها را بررسی کرده و واکنشهایی که ممکن است در این مدت رخ داده باشد را ثبت کنید به عنوان مثال، جابجایی محیط کشت در لوله، تخمیر یا جوشش هنگامی که لولهها به آرامی تکان داده میشوند.
۱۱. لولههایی که گاز منفی (gas-negative) هستند را مجددا به مدت 24 ساعت انکوباسیون کرده و واکنشها را بررسی و ثبت کنید.
۱۲. آزمایش تأیید شده را بر روی کلیه لولههای گاز مثبت احتمالی انجام دهید.
با استفاده از لوپ، از هر لوله LST یا آبگوشت لاکتوز، سوسپانسیون را به لولهای که حاوی آب گوشت BGLB است، منتقل کنید. در صورتی که روی نمونه لایهای ایجاد شده است ابتدا آن را جدا کنید. (از اپلیکاتور استریل نیز ممکن است برای این انتقال استفاده شود).
لولههای BGLB را در دمای 0.5 ± 35 سانتیگراد انکوباسیون کرده و تولید گاز را در 3 ± 48 ساعت بررسی کنید.
محتملترین تعداد (MPN) کلی فرم ها بر اساس نسبت لولههای LST گاز دار تایید شده برای 3 رقت متوالی تعیین میشود.
۵-۳. آزمایش MPN تاییدی برای کلی فرم مدفوعی و E. coli
با استفاده از لوپ، از هر لوله LST یا آبگوشت لاکتوز، سوسپانسیون را به لولهای که حاوی مایع EC است، منتقل کنید. (از اپلیکاتور استریل نیز ممکن است برای این انتقال استفاده شود).
لوله های EC را به مدت 2 ± 24 ساعت در دمای 44.5 درجه سانتیگراد انکوباسیون کنید. سپس لوله را از نظر تولید گاز بررسی کنید.
در صورت منفی بودن، مجدداً لوله را به مدت 2 ± 48 ساعت انکوباسیون کنید. از نتایج این آزمایش برای محاسبه MPN کلی فرم مدفوعی استفاده کنید.
از روش EC broth MPN ممکن است برای آب دریا نیز استفاده شود.
۶-۳. آزمایش MPN تکمیلی برای E. coli
جهت انجام آزمایش تکمیلی برای E. coli ، هر لوله EC گازدار را به آرامی تکان دهید. سپس با استفاده از لوپ یک مقداری از نمونه درون لوله EC را برداشته و آن را روی آگار و L-EMB کشت خطی کنید. سپس پلیت حاوی آگار را به مدت 18 الی 24 ساعت در دمای 0.5 ± 35 درجه سانتی گراد انکوباسیون کنید.
پلیتها را از لحاظ وجود کلنیهای E. coli بررسی کنید. این کار از طریق بررسی مرکز تاریک و صاف و جلای فلزی کلنیها انجام میشود. برای انجام آزمایشهای بیشتر، حداکثر 5 کلنی مشکوک را از هر پلیت حاوی آگار L-EMB به اسلنت کالچر PCA منتقل کنید و آنها را به مدت 18-24 ساعت در دمای 0.5 ± 35 درجه سانتیگراد انکوباسیون کنید.
توجه: در صورتی که از هر 5 کلنی، 1 کلنی به عنوان E. coli شناسایی شود، میتوان آن لولهی EC را مثبت دانست و دیگر نیازی نیست که هر 5 کلنی مورد آزمایش قرار بگیرند.
رنگ آمیزی گرم را انجام دهید. تمام کشتهایی که در آنها میکروارگانیسمها به صورت گرم منفی و میلهای کوتاه به نظر میرسند، باید از نظر واکنشهای IMViC که در ادامه مطرح شده است، آزمایش شوند و همچنین برای تأیید تولید گاز مجدداً در آگار LST تلقیح شوند. آزمایش IMViC جهت شناسایی و تمایز گونههای انتروباکتریاسه مورد استفاده قرار میگیرند که حرف I اول کلمه ایندول، حرف M از اول کلمه متیلرد، حرف V از اول کلمه ووگس-پروسکوئر و حرف C از کلمه سیترات گرفته شده است و حرف i برای بیان راحتتر این واژه است.
۷-۳. آزمایش IMViC
- ایندول: نمونه را درون لوله حاوی آبگوشت تریپتون تلقیح کنید و به مدت 2 ± 24 ساعت در دمای 0.5 ± 35 درجه سانتیگراد انکوباسیون کنید. با افزودن 0.2 الی 0.3 میلی لیتر از معرف Kovacs، ایندول را آزمایش کنید. ظاهر شدن رنگ قرمز در لایه فوقانی بیانگر نتیجه مثبت است.
- ترکیبات واکنش دهنده ووگس-پروسکوئر: نمونه را درون لوله حاوی آبگوشت MR-VP تلقیح کرده و 2 ± 48 ساعت در دمای 0.5 ± 35 درجه سانتیگراد انکوباسیون کنید. 1 میلی لیتر از این ماده را به یک لوله آزمایش لوله ۱۰۰ × ۱۳ منتقل کنید. 0.6 میلی لیتر محلول α-نفتول و 0.2 میلی لیتر 40٪ KOH را به لوله اضافه کنید و لوله را تکان دهید. مقداری کریستال کراتین اضافه کنید. لوله را روی شیکر لوله قرار داده و اجازه دهید 2 ساعت بماند. اگر رنگ صورتی ائوزین ایجاد شود، آزمایش مثبت است.
- متیل رد: بعد از آزمایش ووگس-پروسکوئر، لولههای MR-VP را به مدت 2 ± 48 ساعت در دمای 0.5 ± 35 درجه سانتیگراد انکوباسیون کنید. به هر لوله 5 قطره محلول متیل رد اضافه کنید. رنگ قرمز بیانگر نتیجه آزمون مثبت است. رنگ زرد واکنش منفی را نشان میدهد.
- سیترات: نمونه را درون لوله حاوی سیترات کوثر به آرامی تلقیح کنید. سعی کنید مایع کدر نشود. لوله را به مدت 96 ساعت در دمای 0.5 ± 35 درجه سانتیگراد انکوباسیون کنید. ایجاد کدورت واکنش مثبت را نشان میدهد.
- گاز حاصل از تخمیر لاکتوز.:یک لوله LST را تلقیح کرده و در دمای 0.5 ± 35 درجه سانتیگراد به مدت 2 ± 48 ساعت انکوباسیون کنید. تولید گاز (جابجایی محیط از داخل لوله) یا جوشش بعد از هم زدن ملایم، واکنش مثبت را نشان میدهد.
تفسیر نتایج برای تشخیص مثبت باکتری اشریشیا کلی به صورت زیر است:
(الف) ظرف 48 ساعت در 35 درجه سانتیگراد تخمیر لاکتوز رخ داده و درون لوله گاز ایجاد میشود.
(ب) میکروارگانیسمها به صورت میلههای گرم منفی بدون اسپور ظاهر میشوند.
(ج) الگوهای IMViC به صورت ++ – (بیوتیپ 1) یا – + – (بیوتیپ 2) هستند.
۸-۳. استفاده از محیط کشت جامد برای کلی فرم
- آگار لاکتوز صفراوی بنفش قرمز (VRBA) را طبق دستورالعمل سازنده تهیه کنید. توجه داشته باشید که قبل از استفاده تا 48 درجه سانتیگراد سرد شود. نمونهای را که در بخش 3-3 توضیح داده شده آماده، همگن و رقیق کنید تا کلنیهای ایزوله حاصل شوند.
- 2 میلی لیتر از هر رقت را به 2 پتری دیش منتقل کنید.
- 10 میلی لیتر VRBA که به دمای 48 درجه سانتیگراد رسیده است را درون پتری دیشها بریزید. پتری دیش را به آرامی تکان دهید تا با نمونه مخلوط شود و اجازه دهید تا آگار جامد شود.
- برای جلوگیری از رشد سطحی و گسترش کلنیها، پتری دیش را با 5 میلی لیتر VRBA بپوشانید و مجددا اجازه دهید تا جامد شود.
- در صورت نیاز به احیا، یک لایه پایه 8 الی10 میلی لیتری از آگار تریپتیک سویا که به دمای 48 درجه سانتیگراد رسیده است را درون ظروف بریزید.
- پتری دیش را کمی بچرخانید تا نمونهها مخلوط شوند و در دمای اتاق به مدت 0.5 ±2 ساعت انکوباسیون کنید. سپس 8 الی10 میلی لیتر VRBA ذوب شده و خنک شده روی آن قرار دهید و اجازه دهید تا جامد شود.
- پتری دیشها را معکوس کرده و 18-24 ساعت در دمای 35 درجه سانتیگراد انکوباسیون کنید. توجه داشته باشید که محصولات لبنی را در دمای 32 درجه سانتیگراد انکوباسیون نمایید.
- پتری دیش را زیر میکروسکوپ بررسی کنید. کلنیهای قرمز مایل به بنفش که دارای قطر 0/5 میلیمتر یا بیشتر هستند و توسط منطقهای از اسیدهای صفراوی رسوب شده احاطه شدهاند، را بشمارید.
- هر پتری دیش باید حدودا حاوی 25 الی250 کلنی باشد. برای تأیید کلی فرم بودن کلنیها، حداقل 10 کلنی نماینده انتخاب کنید و هر کدام را به یک لوله حاوی آبگوشت BGLB منتقل کنید.
- لوله ها را در دمای 35 درجه سانتیگراد انکوباسیون کنید و هریک را از نظر تولید گاز پس از 24 و 48 ساعت بررسی نمایید.
توجه: اگر نتیجه بررسی لوله BGLB گاز مثبت بود، لازم است رنگآمیزی گرم صورت گیرد. زیرا این نتیجه میتواند در اثر تخمیر لاکتوز توسط باکتریهای گرم مثبت موجود در نمونه نیز ایجاد شود.
متناوباً، کلنی های E. coli را نیز می توان با افزودن 100 میکروگرم 4methyl-umbelliferyl-β-D-glucuronide در هر میلی لیتر از VRBA در میان کلنیهای کلی فرم تشخیص داد. با این کار، پس از انکوباسیونِ نمونه، با استفاده از اشعه UV موج بلند، فلورسانس مایل به آبی در اطراف کلنیها قابل مشاهده است.
۴. روش LST-MUG برای تشخیص E. coli در غذاهای سرد یا منجمد
روش LST-MUG بر اساس فعالیت آنزیمی به نام β-گلوکورونیداز (GUD) است که باعث بستن بستر 4-methylumbelliferyl β-D-glucuronide یا به اصطلاح MUG میشود تا 4-متیل آمبولی فرون (MU) آزاد شود.
با قرار گرفتن در معرض اشعه ماورا بنفش با امواج طولانی (365 نانومتر) ، MU یک فلورسانس مایل به آبی را نشان میدهد که به راحتی در محیط کشت یا اطراف کلنیها قابل مشاهده است.
بیش از 95٪ گونههای اشریشیا کلی از جمله سویههای بی هوازی (غیر تولید کننده گاز) GUD تولید میکنند.
یک استثنا اشریشیا کلی انتروهموراژیک (EHEC) است که به طور مداوم GUD منفی است. کمبود فنوتیپ GUD اغلب برای تمایز این سروتیپ از سایر سروتیپهای اشریشیا کلی استفاده میشود.
تولید GUD توسط سایر اعضای خانواده انتروباکتریاسیا نادر است، به استثنای برخی از گونههای شیگلا (44 -58%) و سالمونلا (20-29%).
برای تشخیص باکتری اشریشیا کلی، MUGرا میتوان تقریباً در هر محیط کشتی استفاده کرد .اما برخی از محیط کشتها مانند EMB که حاوی اجزای فلورسنت هستند، مناسب نیستند، زیرا باعث پوشیده شدن فلورسانس MU خواهند شد.
هنگامی که MUG در محیط LST گنجانده میشود، می توان فرم های کلی فرم را بر اساس تولید گاز در اثر تخمیر لاکتوز برشمرد و E. coli نیز توسط فلورسانس در محیط کشتی که تحت اشعه UV موج بلند قرار دارد، شناسایی میشود. بنابراین در این روش یک شناسایی احتمالی E. coli ظرف 24 ساعت رخ خواهد داد.
توجه: برای مشاهده فلورسانس، لولههای LST-MUG تلقیح شده را تحت اشعه UV با امواج طولانی (365 نانومتر) در تاریکی بررسی کنید. یک لامپ ماورا بنفش دستی 6 وات برای انجام این کار کافی است. هنگام استفاده از منبع اشعه ماورا بنفش قویتر، مانند لامپ فلورسنت 15 وات، از عینک محافظ استفاده کنید. همچنین، پیش از انجام روش MUG ، تمام لولههای شیشهای را از نظر فلورسانس بررسی کنید. اکسید سریم (Cerium oxide)، که بعضاً برای کنترل کیفیت به شیشه اضافه میشود، زیر نور ماورا بنفش فلورسانس میشود و در آزمایش MUG تداخل ایجاد میکند. همچنین توجه داشته باشید که استفاده از سویههای کنترل مثبت و منفی برای واکنش MUG ضروری است.
۱-۴. تجهیزات و مواد
به بخش 3-1 در بالا مراجعه کنید. علاوه بر تجهیزات ذکر شده در قسمت A به موارد زیر نیز احتیاج دارید:
- لولههای شیشهای بوروسیلیکات یکبار مصرف (100 × 16)
- لولههای Durham از جنش شیشه بوروسیلیکات (50 × 9) برای جمع آوری گاز
- لامپ UV امواج طولانی، بیش از 6 وات نباشد
۲-۴. محیط کشت و معرفها
معرفها و محیط کشتهایی که برای انجام این آزمایش مورد استفاده قرار میگیرند پیشتر در قسمت 3-2 بیان شدهاند.
۳-۴. آزمایش احتمالی LST-MUG برای E. coli
- نمونههای غذایی را تهیه کنید و آزمایش پیش فرض MPN را همانطور که در بخش 3-3 توضیح داده شده است، انجام دهید. با این تفاوت که بهجای لولههای LST از لولههایLST-MUG استفاده کنید.
- یک لوله LST-MUG را با یک کلنی GUD مثبت coli به عنوان شاهد مثبت تلقیح کنید.
- همچنین یک لوله دیگر را با کشت کلبسیلا پنومونیه یا انتروباکتر آئروژنز به عنوان کنترل منفی تلقیح کنید تا تمایز لولههای نمونه از نظر رشد ارگانیسم و فلورسانس تسهیل شود.
- لولهها را به مدت 24 تا 48 ساعت (۲ ± ساعت) در دمای 35 درجه سانتیگراد انکوباسیون کنید. هر لوله را از نظر رشد میکروارگانیسم و ایجاد کدورت یا گاز بررسی کنید. سپس لولهها را در تاریکی و با استفاده از لامپ UV موج بلند (365 نانومتر) بررسی کنید. مشاهدهی فلورسانس مایل به آبی یک آزمایش احتمالی مثبت برای coli است.
مطالعات صورت گرفته نشان میدهد که مشاهده فلورسانس آبی پس از 24 ساعت انکوباسیون پیش بینی دقیقی برای حضور E. coli در نمونه است و میتواند 83 الی95٪ از لولههای E. coli مثبت را شناسایی کند. پس از 48 ساعت انکوباسیون، 96 الی 100٪ لولههای E. coli مثبت قابل شناسایی هستند.
برای انجام آزمایش تاییدی، یک لوپ استریل را به ماده درون لوله فلورسانس آغشته کرده و به آگار L-EMB منتقل کنید. سپس لولهها را به مدت 2±24 ساعت در دمای 35 درجه سانتیگراد انکوباسیون کنید. توجه داشته باشید که آزمایش تأیید شده را روی همه لولههای مثبت انجام دهید.
برای انجام تست کامل E. coli پروتکل های ذکر شده در بخش 3-6 را دنبال کنید.MPN E. coli بر اساس ترکیبی از لولههای فلورسانس تایید شده در 3 رقت متوالی محاسبه میشود.
۵. بررسی آب بطری
مصرف آب بطری به سرعت در سراسر جهان در حال افزایش است.
سازمان غذا و داروی آمریکا آب بطری را به این صورت تعریف میکند: “آبی که برای مصرف انسان در نظر گرفته میشود و در بطریها یا ظروف دیگر بدون مواد افزودنی بستهبندی میشود که ممکن است حاوی مواد ضد میکروبی ایمن و مناسبی باشد. همچنین ممکن است با رعایت محدودیتهای تعیین شده مقداری فلوراید نیز به آن اضافه شود.
آب بطری ممکن است به عنوان یک نوشیدنی یا به عنوان یک ماده موثر در سایر نوشیدنیها استفاده شود.
ارگانیسمهای کلی فرم لزوما پاتوژنِ بیماریزا نیستند و بهندرت در آب بطری یافت میشوند. با این وجود، به عنوان شاخصی از آلودگی یا آلودگی احتمالی در نظر گرفته میشوند. بررسی ها نشان داده است كه در اغلب موارد كلیفرمها شاخصهای كیفیت آب بطری هستند، اما بعضی از كشورها جمعیت میكروبی دیگری را به عنوان شاخص كیفیت آب بطری كنترل میكنند. طبق استاندارد فعلی کیفیت آب بطری شده، FDA کنترل کیفیت میکروبیولوژیکی بطری آب را براساس تشخیص میزان کلی فرم تعیین کرده است. این میزان ممکن است با فیلتراسیون غشایی (MF) یا با تجزیه و تحلیل 10 لولهیMPN از 10 واحد تحلیلی 10 میلی لیتری بهدست آید.
۱-۵. تجهیزات و مواد
- دستگاه انکوباتور 0.5 ± 35 درجه سانتی گراد
- تجهیزات فیلتراسیون غشایی (پایه فیلتر و قیفها): از جنس شیشه، پلاستیک یا فولاد ضد زنگ که در فویل یا کاغذ پیچیده و استریل میشود.
- محفظه استریل کننده ماورا بنفش برای استریل کردن پایه و فانل فیلتر (اختیاری).
- فلاسک خلاء برای نگه داشتن فانل فیلتر
- منبع خلا (پمپ خلا electric الکتریکی یا water aspirator).
- فیلترهای غشایی استریل، سفید، مشبک با قطر 47 میلی متر، اندازه منافذ 0.45 میکرومتر برای شمارش باکتریها.
- پتری دیش استریل، از جنس پلاستیک، با 50 × 12 میلی متر، با دربهای محکم.
- پنس برای انتقال غشاها و جلوگیری از آسیب دیدن آنها
۲-۵. محیط کشتها
- آبگوشت تریپتوز لوریل سولفات (LST)
- محیط کشت برلیانت گرین براث (BGLB)
- محیط کشت ام-اندو آگار (M-Endo Medium)
- LES-Endo Agar
۳-۵. تست کولیفرم 10 لوله MPN – روشهای فرضی و تأیید شده
- برای بررسی معمول آب بطری، 100 میلی لیتر از نمونه را بردارید ونمونهی رقیق نشده را درون 10 لوله 2X LST (حاوی 10 میلی لیتر از محیط کشت) تلقیح کنید. درون هر لوله 10 میلی لیتر از نمونه بریزید. لولهها را در دمای 35 درجه سانتیگراد انکوباسیون کنید.
- لولهها را پس از گذشت 2 ± 24 ساعت از نظر تشکیل گاز بررسی کنید. تشکیل گاز با جابجایی محیط در ویال یا جوشش هنگامی که لولهها به آرامی تحریک میشوند، مشخص میگردد.
- در صورت منفی بودن تشکیل گاز در 24 ساعت، مجددا لولهها را برای 24 ساعت اضافی انکوباسیون کرده و از نظر تولید گاز بررسی کنید.
- جهت انجام آزمایش تاییدی بر روی تمامی لولههای احتمالی مثبت به شرح زیر اقدام نمایید:
- یک لوله LST مثبت را به آرامی تحریک کرده و با استفاده از لوپ استریل 3 الی 5/3 میلی متر، سوسپانسیون را به یک لوله حاوی آبگوشت BGLB منتقل کنید.
- میتوان از اپلیکاتور استریل برای انتقال استفاده کرد. حداقل 2.5 سانتی متر از اپلیکاتور را در محیط فرو ببرید. لولههای BGLB را به مدت 2 ± 48 ساعت در دمای 35 درجه سانتیگراد انکوباسیون کنید.
- لولهها را از نظر تولید گاز بررسی کنید.
اگر مشخص شد که نمونهای حاوی کلی فرم (در هر سطح) است، برای تعیین E. coli طبق روال مشخص شده در بخش3-6 در بالا عمل کنید. آب بطری حاوی E. coli مجاز نیست.
۴-۵. روش فیلتر غشایی برای کلی فرمها
- 100 میلی لیتر نمونه آزمایش را فیلتر کرده و فیلتر را به محیط M-Endo یا LES Endo Agar منتقل کنید. نمونه را در دمای 0.5 ± 35 درجه سانتیگراد به مدت 22 الی24 ساعت انکوباسیون کنید.
- کلنیهایی که از رنگ صورتی تا قرمز تیره هستند و دارای جلای فلزی سبز میباشند را بشمارید.
- توجه داشته باشید که جلای فلزی ممکن است از نقاط مشخصی باشد و یا کلنی را پوشش دهد.
- توصیه میشود برای بررسی فیلترها از میکروسکوپ نوع کالبد شکافی استفاده کنید.
جهت تایید کلنیها به صورت زیر عمل کنید:
- اگر 5 تا 10 کلنی براق بر روی فیلتر وجود دارد، تمام کلنیها را در لوله های LST تلقیح کنید. سپس لولهها را در دمای 0.5 ± 35 درجه سانتیگراد به مدت 48 ساعت انکوباسیون کنید.
- اگر تعداد کلنیهای براق از 10 بیشتر است، به طور تصادفی 10 کلنی را انتخاب کنید. این 10 کلنی نمایانگر همه کلنیهای دارای جلای فلزی هستند.
- در صورت گاز مثبت بودن لولههای LST، نمونهی موجود در هر لوله باید در محیط کشت BGLB تلقیح شده و به مدت 48 ساعت در دمای انکوباسیون گردد. تولید گاز در BGLB طی 48 ساعت یک آزمایش کلی فرم مثبت است.
- نتایج را به عنوان تعداد کلنیهای کلی فرم در هر 100 میلی لیتر ثبت کنید
توجه: روش استاندارد امکان تلقیح همزمان LST و BGLB را هنگام تأیید فراهم میکند. با این وجود، BGLB تا حدودی بازدارنده است بنابراین روشی که در بالا توضیح داده شد که در آن نمونه ها از LST به BGLB زیر کشت میشوند به عنوان یک روش تأیید حساستر در نظر گرفته میشود و بنابراین توصیه میگردد.
- اگر مشخص شد که نمونهای حاوی کلی فرم (در هر سطح) است، برای تعیین coli طبق روال مشخص شده در بخش 3-6 در بالا عمل کنید. آب بطری حاوی E. coli مجاز نیست.
۶. بررسی E. coli در آب مرکبات
آزمایشات شناسایی اشریشیا کلی برای بررسی آب مرکبات آلوده و یا بررسی اثربخشی سیستم کنترل نقطه بحرانی تجزیه و تحلیل خطر (HACCP) در طی فرآوری آب مرکبات انجام میشود.
روش استانداردی که معمولاً برای آزمایش باکتری اشریشیا کلی استفاده میشود، روش MPN است، اما به دلیل اسیدیته (pH 3.6 to 4.3) آب مرکبات، که میتواند در آزمایش تداخل ایجاد کند، به نظر میرسد که این روش کارامد نیست.
برخلاف اکثر روشهای شناسایی E. coli، که سنجشی هستند، روش زیر یک آزمایش ساده حضور و غیاب (Presence/Absence test) است که به کمک آن میتوان حجم 10 میلی لیتر آب میوه را بررسی کرد.
این روش، که به عنوان روش اصلاح شده ColiComplete (CC) تعیین شده است، از MUG برای تشخیص E. coli استفاده میکند.
۱-۶. تجهیزات و مواد
- حمام آب پوشیده، دارای سیستم سیرکولاسیون برای حفظ دمای 0.2 ± 44.5 درجه سانتیگراد.
- انکوباتور درجه سانتیگراد 0.5 ± 35
- نور ماورا بنفش Longwave [حدود 365 نانومتر] . بیش از 6 وات نباشد.
۲-۶. محیط کشت و معرف ها
- محیط کشت Universal Preenrichment Broth (UPEB)
- محیط EC
- دیسک های ColiComplete (CC)
۳-۶. تهیه، غنی سازی و تجزیه و تحلیل نمونه
- دو نمونه را به روش زیر آماده کنید.
- با استفاده از تکنیک آسپتیک، مقدار 10 میلی لیتر آب مرکبات را در 90 میلی لیتر از محیط کشت UPEB تلقیح کرده و در دمای 0.5 ± 35 به مدت 24 ساعت انکوباسیون کنید.
- پس از غنی سازی، 1 میلی لیتر از هر آبگوشت UPEB را به 9 میلی لیتر آبگوشت EC حاوی دیسک CC منتقل کنید.
- لولههای حاوی EC / CC را در دمای 0.2 ± 44.5 درجه سانتیگراد در یک حمام آب دارای سیستم سیرکولاسیون به مدت 2 ±24 ساعت انکوباسیون کنید.
- سویه MUG (+) E. coli را به عنوان شاهد مثبت و دیگری را با کلبسیلا پنومونیه یا انتروباکتر آئروژنز به عنوان شاهد منفی به نمونه اضافه کنید.
- لوله ها را در تاریکی و زیر نور UV با موج طولانی بررسی کنید. وجود فلورسانس آبی در هر یک از لولهها نشان دهنده وجود coli در نمونه است.
- توجه: دیسکهای CC همچنین حاوی X-gal هستند که در صورت شکافتن توسط بتا-گالاکتوزیداز (β-galactosidase)، رنگ آبی روی دیسک یا اطراف آن ایجاد میشود. این واکنش مشابه اندازهگیری میزان تولید اسید / گاز از تخمیر لاکتوز است، از این رو وجود رنگ آبی نشان دهنده کلی فرم مثبت است.
۷. جمعبندی
روشهای زیادی برای شمارش کلی فرمها و باکتری اشریشیا کلی در آب و مواد غذایی وجود دارد. به عنوان مثال روشهای مختلفی که از نشانگرهای فلوروژنیک مانند MUG یا سایر سوبستراهای کروموژنیک برای تشخیص و شناسایی کلیفرم و E. coli در غذاها استفاده میکنند.
در این مطلب سعی کردیم یکی از تکنیکهای رایج برای شناسایی کلیفرمها و باکتری اشریشیا کلی در صنایع غذایی را بیان کنیم.
همانطور که در ابتدای مطلب نیز گفته شد، کلی فرمها و همچنین باکتری اشریشیا کلی ممکن است بیماریزا تلقی نشوند اما به عنوان شاخصی برای آلودگی مواد غذایی در نظر گرفته میشوند.
امیدواریم این مطلب مورد توجه شما قرار گرفته باشد.





سلام خداقوت خیلی جذاب بود سپاسگزارم از اینکه این محتوای خفن برامون به اشتراک گذاشتی خیلی باحالی دمت چیپس